Pseudohypoparatyreóza typu Ib: kazuistika a literárny prehľad
Pseudohypoparathyroidism type Ib: a case report and review of literature
Pseudohypoparathyroidism (PHP) is a group of rare hereditary diseases caused by tissue resistance to parathyroid hormone (PTH), there are two main types I and II. Type I is divided into subtypes. The authors present a case of PHP Ib with hypocalcemia accidentally detected at childbirth. After the unsuccessful treatment of hypocalcemia, the etiology was considered. Although PHP was considered and treatment was tried, the confirmation of the diagnosis and the treatment were not adequately tightened. Years later, PHP Ib has been genetically confirmed. By adjusting the treatment, the difficulties subsided and the effect of PTH on bone was reduced, which is expected to improve the prognosis to the level of the population.
Keywords:
hyperphosphatemia – hypocalcemia – Parathyroid hormone – pseudohypoparathyroidism
Vyšlo v časopise:
Clinical Osteology 2021; 26(1): 39-43
Kategorie:
Kazuistiky
Souhrn
Pseudohypoparatyreóza (PHP) je skupina raritných vrodených ochorení spôsobená rezistenciou tkanív na parathormón (PTH), ktoré delíme na I a II typ. Typ I sa člení na podtypy. Autori prezentujú prípad PHP Ib s náhodne pri pôrode zachytenou hypokalciémiou. Po neúspešnej liečbe hypokalciémie sa začalo uvažovať o príčine. Aj keď sa na PHP myslelo a liečba bola skusmo zahájená, potvrdenie diagnózy a liečba neboli adekvátne dotiahnuté. Po rokoch bola PHP Ib potvrdená geneticky. Úpravou liečby došlo k ústupu ťažkostí a zníženiu účinku PTH na kosť, čím sa predpokladá zlepšenie prognózy na úroveň populácie.
Klíčová slova:
hyperfosfatémia – hypokalciémia – parathormon – pseudohypoparatyreóza
Úvod
Idiopatické a dedičné formy rôzneho stupňa rezistencie na parathormón sú označované ako pseudohypoparatyreóza. Ide o skupinu rozmanitých ochorení, u ktorých sa v dôsledku rezistencie na parathormón, mechanizmom spätnej väzby, zvyšuje sekrécia parathormónu, no napriek tomu pretrváva hypokalciémia a hyperfosfatémia s potrebou doživotnej suplementácie vápnika a aktívnej formy vitamínu D. Pre niektorých pacientov je charakteristický špecifický fenotyp Albrightovej hereditárnej osteodystrofie (AHO). Na základe biochemických a molekulárnych analýz rozdeľujeme pseudohypoparatyreózu na dva hlavné typy I a II. Typ I sa člení na ďalšie podtypy. Väčšina týchto ochorení je diagnostikovaná v detskom veku [1]. Pri sporadickej pseudohypoparatyreóze Ib to až tak neplatí, pretože k rozvoju klinických príznakov dochádza až v priebehu života a pacienti nemajú výraznejšie prejavy Albrightovej hereditárnej osteodystrofie. Skutočná prevalencia ochorenia nie je známa [2]. Dáta publikované z Japonska hovoria o prevalencii 0,34 na 100 000 [3], z Dánska 1,1 na 100 000 osôb [1]. Príčinou ochorenia je molekulárny defekt na úrovni receptora spôsobený narušením signálnej dráhy v oblasti alfa podjednotky stimulačného G-proteínu, ktorého úlohou je aktivácia adenylátcyklázy (cAMP) [4]. V patogenéze sa uplatňujú sporadické alebo autosomálne dominantné vrodené genetické mutácie, alebo epigenetické zmeny zahrňujúce GNAS génový lokus na chromozóme 20q13.3 [5]. GNAS lokus kóduje alfa podjednotku stimulačného G proteínu (Gs), ktorý je hlavným regulátorom cAMP signálnej dráhy [2]. Prvýkrát prípad rezistencie na parathormón opísal a zdokumentoval americký endokrinológ Fuller Albright v roku 1942. Súbor pacientov mal nízky vzrast, guľatú tvár, skrátený štvrtý metakarp a ďalšie metakarpálne kosti, centrálnu obezitu, podkožné kalcifikácie a rôzne stupne mentálnej retardácie, zároveň boli pacienti hypokalciemickí a hyperfosfatemickí [6,7]. Tieto heterogénne klinické prejavy sú špecifické pre fenotyp, ktorý bol pomenovaný ako Albrightova hereditárna osteodystrofia. Experimentálne pokusy o podávanie syntetického parathormónu (PTH) u týchto pacientov neviedlo ku zvýšeniu sérového vápnika a nedokázalo vyvolať ani zvýšenú fosfátovú diurézu. Neskôr sa dokázalo, že u pacientov s hypokalciémiou, zvýšenou hladinou PTH a črtami Albrightovej hereditárnej osteodystrofie, infúzne podanie syntetického PTH nestimulovalo obličkovú produkciu cAMP, čo viedlo k úvahe o defekte v receptore pre PTH alebo v signálnej dráhe adenylcyklázového systému (cAMP signálna dráha) [8]. V minulosti sa rezistencia na PTH určovala pomocou merania cAMP a fosfátúrie po podaní infúzie s PTH (Ellsworthov-Howardov test) [9,10]. Test je už v súčasnej dobe skôr experimentálnou metódou, v bežnej klinickej praxi sa z praktických dôvodov nepoužíva. Ako už bolo spomenuté, pseudohypoparatyreózu rozdeľujeme na dva hlavné typy. Prvý typ je charakterizovaný zníženou odpoveďou adenylcyklázového systému (cAMP a fosfátúrie) na podanie syntetického parathormónu. Pri druhom type je odpoveď cAMP zachovaná, resp. normálna, ale odpoveď fosfátúrie je znížená. Výrazná variabilita klinického obrazu a obličkovej rezistencie na PTH viedla k rozčleneniu pseudohypoparatyreózy na ďalšie podtypy (tab. 1).
![Klasifikácia pseudohypoparatyreózy. Upravené podľa [11]](https://www.clinicalosteology.org/media/cache/resolve/media_object_image_small/media/image_pdf/9b5bac2ec005ad229cd65413539dcce1.png)
Autori prezentujú prípad pacientky s miernou klinickou symptomatológiou, hypokalciémiou pri výrazne zvýšenej hladine parathormónu.
Kazuistika
Prezentovaná pacientka bola od veku 24 rokov sledovaná a liečená v spádovej endokrinologickej ambulancii pre primárnu hypotyreózu na podklade chronickej autoimunitnej tyreoiditídy. V 26 rokoch, počas prvého pôrodu, bola u pacientky na gynekologicko-pôrodníckom oddelení náhodne zachytená výrazná hypokalciémia (1,41 mmol/l), v tom čase bez výraznejšej klinickej symptomatológie. Pôrod prebehol bez komplikácie. Spätne anamnesticky bola u pacientky zistená viacročná, klinicky nešpecifická symptomatológia (palpitácie, celkový tremor). Nadväzné vyšetrenia odhalili vysokú hodnotu PTH (362,0 pg/ml). Diferenciálno-diagnosticky sa vyslovilo podozrenie aj na pseudohypoparatyreózu, no v ďalších vyšetrovacích postupoch sa už nepokračovalo a diagnostika nebola adekvátne dotiahnutá. Do liečby bol pridaný preparát kalcia (1 000 mg p.o. 3-krát denne) v kombinácii s kalcitriolom (0,25 μg p.o. 1-krát denne) a pacientka bola naďalej sledovaná v spádovej endokrinologickej ambulancii. V priebehu nasledujúcich 3 rokov bola opakovane ošetrená na internej ambulancii a ambulancii urgentného príjmu pre neúspešne suplementovanú hypokalciémiu a hyperfosfatémiu so sprievodnou symptomatológiou (palpitácie, celkový tremor, parestézie horných končatín). Pre recidivujúcu symptomatológiu bolo doplnené i psychiatrické vyšetrenie, ktoré stav hodnotilo ako úzkostnú a subdepresívnu poruchu s následným zahájením medikamentóznej liečby. U nás bola vyšetrená ako 29-ročná pre chronickú hypokalciémiu a recidivujúce ťažkosti. Fyziognomicky, v porovnaní s rodičmi, je pacientka nižšieho vzrastu, BMI: 19,52 kg/m2, fyzikálne vyšetrenie neodhalilo žiadnu patológiu, ktorá by poukazovala na toto ochorenie. Pacientka bola bez prejavov Albrightovej hereditárnej osteodystrofie. Anamnesticky sme familiárny výskyt vrodených vývojových chýb, eventuálne iných závažných, geneticky podmienených patologických stavov, nezachytili. Vstupné laboratórne výsledky, v tom čase na medikamentóznej liečbe: kalcitriol 0,25 μg p.o. 1-krát denne, uhličitan vápenatý 1 000 mg p.o. 2-krát denne, levotyroxín ob deň 100 a 75 μg, metoprolol 25 mg 2-krát denne, klonazepam 0,25 mg 3-krát denne, escitalopram 5 mg 1-krát denne, vitamín C 250 mg 2-krát denne (tab. 2). Ultrasonografickým (USG) vyšetrením sme prištítne telieska nevizualizovali. Denzitometricky sme potvrdili kostnú denzitu primeranú pre daný vek a pohlavie (tab. 3).
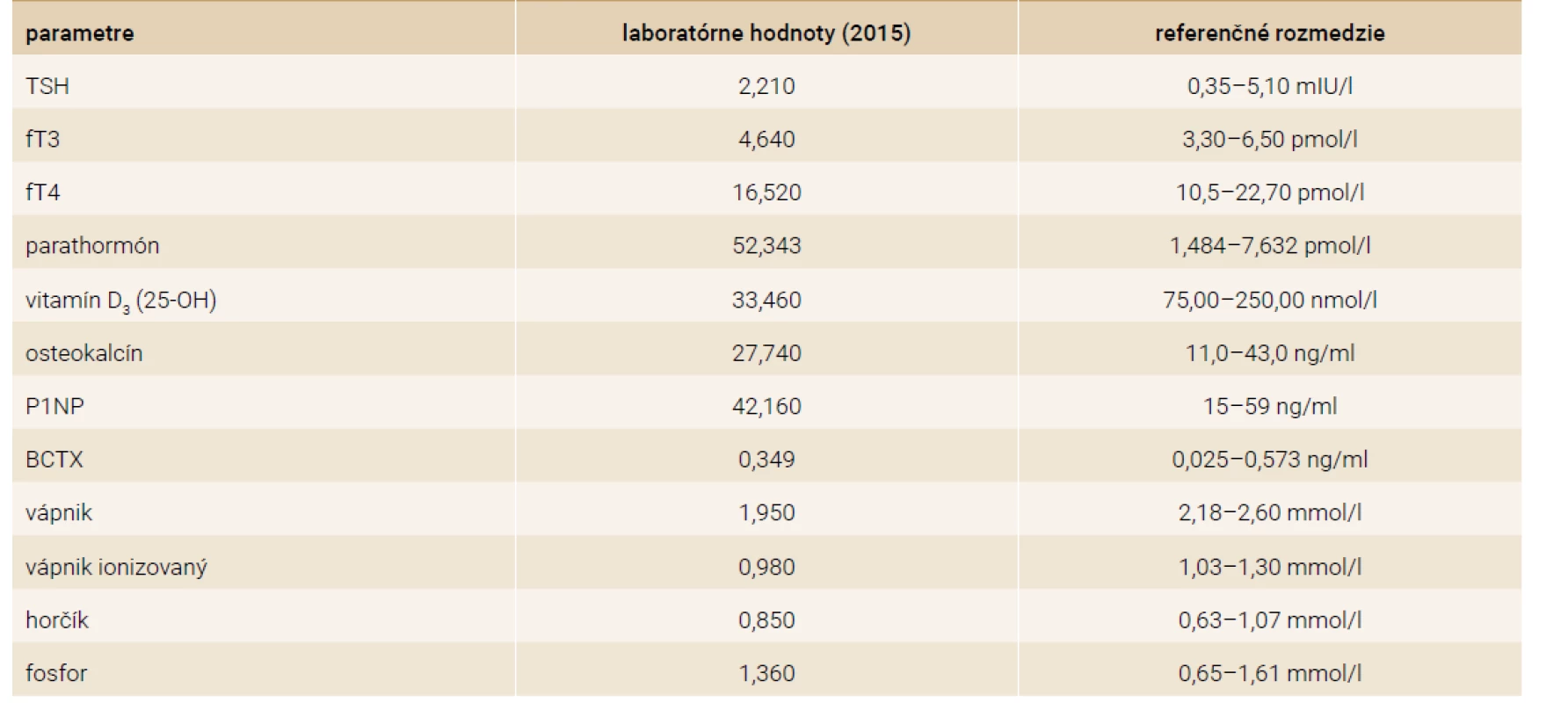
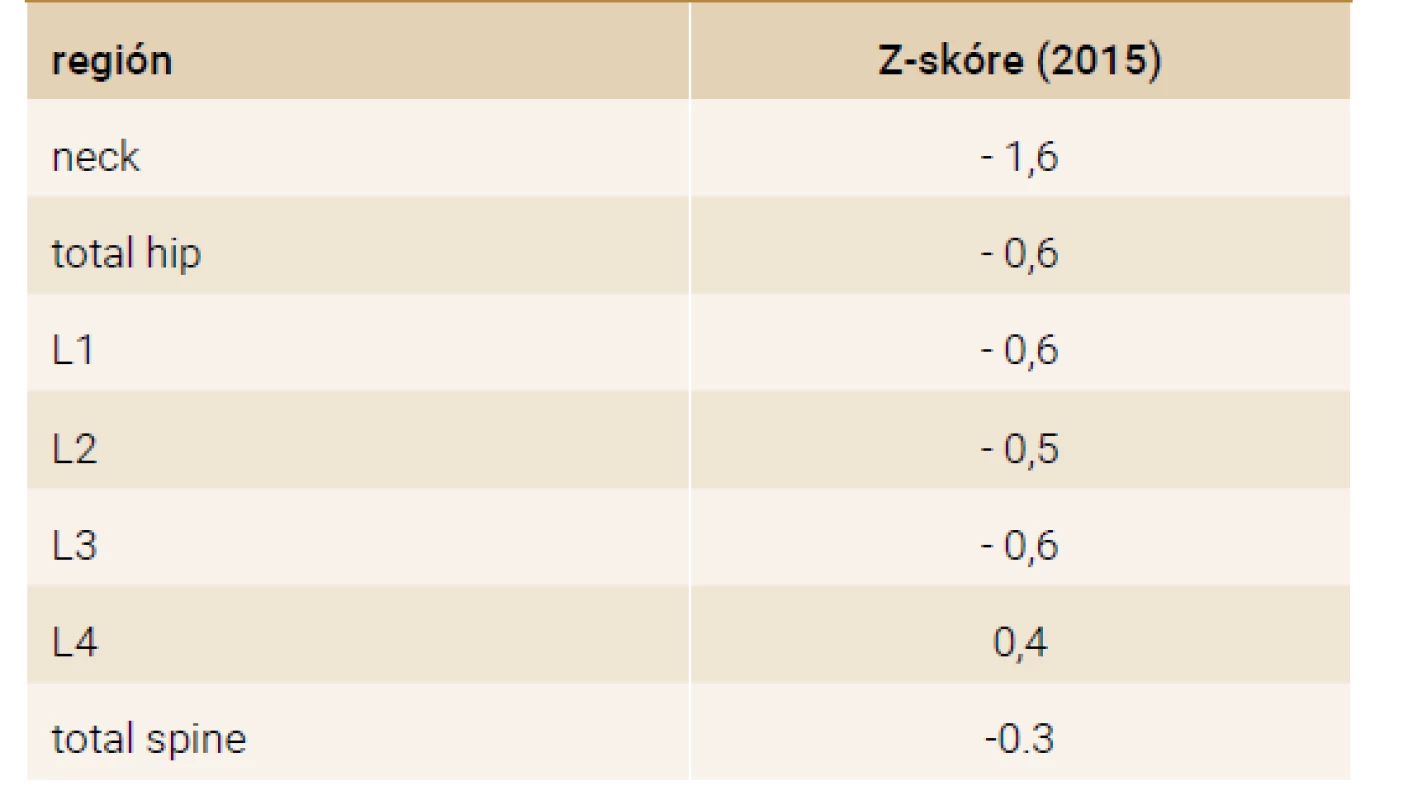
Vzhľadom na pretrvávajúce subjektívne ťažkosti a laboratórny nález sme navýšili dávkovanie kalcitriolu na 0,25 μg p.o. 2-krát denne, uhličitan vápenatý sme znížili na 1 500 mg p.o. denne, deficit vitamínu D sme suplementovali cholekalciferolom v dávke 2 000 IU denne. Pre vysokú suspekciu na pseudohypoparatyreózu sme odobrali krv na genetické vyšetrenie, ktoré potvrdilo extrametyláciu domény NESP55 a stratu metylácie domén NESPAS, GNASXL a GNASA/B. Výsledný metylačný model je pravdepodobne dôsledkom paternálnej uniparentálnej izodisómie, ktorá je považovaná za príčinu sporadickej formy pseudohypoparatyreózy Ib. Po úprave liečby došlo u pacientky ku stabilizácii celkového klinického stavu, s ústupom subjektívnych ťažkostí a postupnému vysadeniu metoprololu, klonazepamu a escitalopramu. Prehľad laboratórnych parametrov na liečbe uvádzame v tabuľke (tab. 4). Napriek pretrvávaniu mierne zvýšenej hodnoty PTH kontrolné denzitometrické vyšetrenia nepotvrdili u pacientky zhoršenie kostnej denzity (tab. 5). Ako 31-ročná pacientka porodila druhé zdravé dieťa, priebeh gravidity a pôrodu bol bez komplikácie.
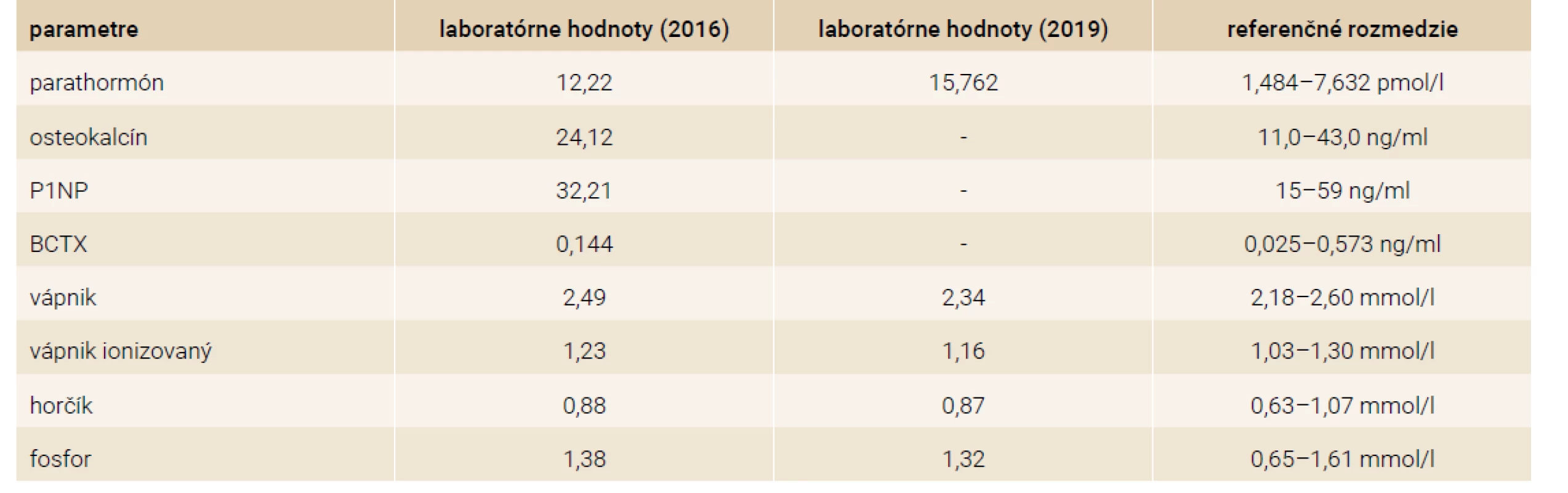
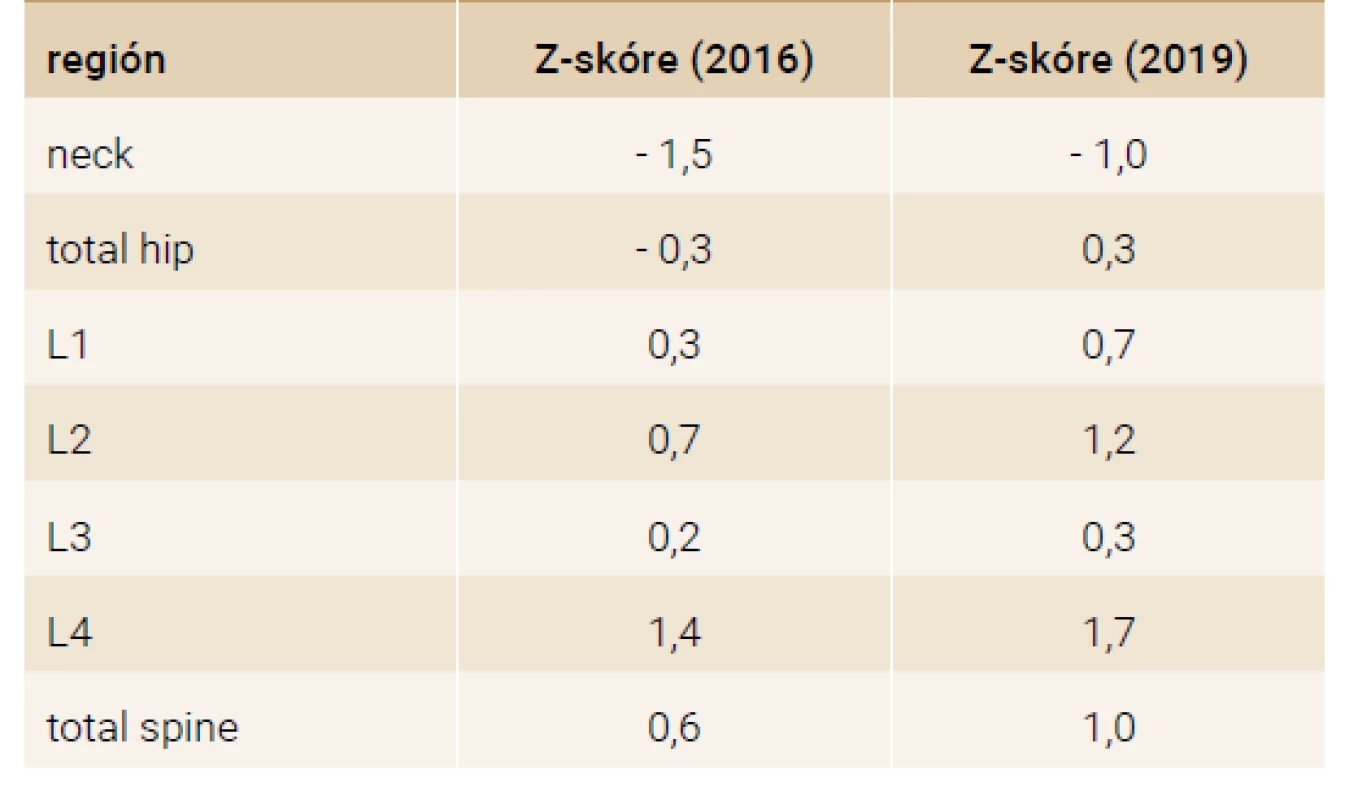
Diskusia
Dlhotrvajúca hypokalciémia s hyperfosfatémiou a výraznou hyperparatyreózou, ktorá pretrvávala aj po suplementácii vitamínu D pri normálnych obličkových parametroch, je vysoko suspektná pre diagnózu pseudohypoparatyreózy. Pacienti so pseudohypoparatyreózou Ib nemajú výrazné prejavy Albrightovej hereditárnej osteodystrofie (AHO), ale môžu mať miernu brachydaktýliu [12,13], tú sme u našej pacientky nediagnostikovali. Diferenciálna diagnostika tohto ochorenia v praxi obyčajne nerobí výraznejšie ťažkosti, hoci hypokalciémia s hyperfosfatémiou je charakteristická aj pre hypoparatyreózu. Diagnózu hypoparatyreózy však vylučuje vysoká hodnota parathormónu. Vysoká hodnota parathormónu je tiež typická pre sekundárnu hyperparatyreózu pri deficite vitamínu D, čo však vylúčime suplementáciou vitamínu D s následným poklesom parathormónu. Diagnózu familiárnej alebo sporadickej formy pseudohypoparatyreózy potvrdí genetické vyšetrenie. U našej pacientky bola potvrdená sporadická forma ochorenia, u ktorej sa predpokladá, že zmeny metylácie DNA sú spôsobené vplyvom enviromentálnych a exogénnych faktorov. Po stanovení diagnózy sa kladie dôraz na adekvátnosť medikamentóznej liečby, ktorá minimalizuje klinické prejavy a komplikácie ochorenia. U 30 až 100 % pacientov s typom Ib môže byť prítomná aj rezistencia na TSH, ktorá môže byť iba mierne nad hornou hranicou normy. [4], tú sme u našej pacientky taktiež vylúčili. Medzi hlavné ciele liečby patrí pokus o udržanie normokalciémie a normofosfatémie bez hyperkalciúrie. Základom terapie je preto podávanie aktívneho vitamínu D (kalcitriolu) a suplementácia vápnika [14], eventuálne podľa potreby suplementácia magnézia. Cieľom liečby je supresia hladiny PTH, pokiaľ to umožňuje hladina vápnika v sére a v moči. Medzinárodný konsenzus pre diagnostiku a manažment pseudohypoparatyreózy z roku 2018 [4] odporúča sledovať sérovú hladinu vápnika a jeho vylučovanie močom každých 6 mesiacov u asymptomatických pacientov, alebo u symptomatických pacientov častejšie, a tiež ak pacienti vyžadujú zvýšené dávkovanie aktívneho vitamínu D, napríklad počas akútneho ochorenia, tehotenstva alebo dojčenia. Doposiaľ neboli hlásené žiadne prípady komplikovaného tehotenstva u žien so sporadickou formou pseudohypoparatyreózy Ib [15] a nie sú dostupné ani žiadne informácie ohľadom laktácie [4]. Uvedené informácie potvrdzuje aj prípad našej pacientky, u ktorej prvá a druhá gravidita s následnou laktáciou prebehla bez akýchkoľvek komplikácií.
Za fyziologických okolností PTH zvyšuje koncentráciu vápnika a znižuje koncentráciu fosfátov v plazme. Pôsobí predovšetkým na kosti, obličky a črevá. V kostiach stimuluje osteolýzu spojenú s uvoľňovaním vápnika a fosfátov do krvnej plazmy. V obličkách zvyšuje reabsorpciu vápnika v distálnom tubule a znižuje reabsorpciu fosfátov v proximálnom a distálnom tubule, čím zvyšuje diurézu fostátov. V obličkách zároveň stimuluje syntézu aktívneho 1,25-dihydroxyvitamínu D (vitamín D3) a spolu s ním podporuje resorpciu vápnika z čreva [16]. U zdravého jedinca sa PTH v tkanivách viaže na receptory plazmatickej membrány a spúšťa kaskádu účinkov signálnej dráhy sprostredkovanú adenylcyklázovým systémom. Pri pseudohypoparatyreóze genetické defekty spôsobujú narušenie signálnej kaskády na rôznych úrovniach, v dôsledku čoho vzniká v niektorých orgánoch rezistencia na PTH. Hlavnou črtou pseudohypoparatyreózy typu Ib je rezistencia na PTH v proximálnom tubule obličky. Na rozdiel od proximálnych tubulov, ktoré vykazujú rezistenciu na PTH, osteoblasty izolované z kosti pacientov so pseudohypoparatyreózou Ib vykazujú normálnu cAMP odpoveď na PTH [17]. Účinok PTH na kosť sa javí ako normálny. To naznačuje, že príčinou hypokalciémie nie je skeletálna rezistencia, ale je dôsledkom renálnej rezistencie na PTH a s ňou spojených nízkych hladín aktívneho 1,25-dihydroxyvitamínu D. Vzhľadom na to, že pacienti so pseudohypoparatyreózou Ib nemajú rezistenciu PTH na skelete, mali by mať realizované denzitometrické vyšetrenie [2,18]. Preto je u týchto pacientov zvýšené riziko tzv. hyperparatyroidnej kosti (sekundárnej osteoporózy), ak ochorenie nie je adekvátne liečené [19]. Prevalencia osteoporózy u pacientov so pseudohypoparatyreózou však nie je známa. U prezentovanej pacientky sme vstupne nepotvrdili patologickú zmenu kostnej denzity, napriek vyššej hladine PTH bola primeraná pre daný vek a pohlavie. Je nutné však pripomenúť, že v čase vyšetrenia u nás bola už pacientka liečená preparátom vápnika a kalcitriolom, čo by mohlo čiastočne vysvetľovať fyziologickú kostnú denzitu. Kontrolné denzitometrické vyšetrenia nepotvrdili zhoršenie kostnej denzity i napriek pretrvávaniu ľahko zvýšených hodnôt PTH pri normokalciémii, normofosfatémii a normomagnezémii. V literatúre bol popísaný aj jeden prípad osteosarkómu u pacienta so pseudohypoparatyreózou Ib [20], tento prípad však neposkytuje dostatočné dáta, ktoré by odporúčali špecifický skríning tohto malígneho ochorenia.
V prípade, ak sa u pacientov so pseudohypoparatyreózou objavia neurologické príznaky, je vhodné doplniť CT-vyšetrenie mozgu za účelom vylúčenia intrakraniálnych kalcifikácií. Pacienti by taktiež mali podstúpiť očné vyšetrenie za účelom vylúčenia katarakty a vyšetrenie chrupu [4].
Záver
Keďže pseudohypoparatyreóza patrí medzi raritné ochorenie, doposiaľ neboli realizované žiadne prospektívne klinické štúdie zamerané na manažment a výsledky liečby. Preto manažment a liečba týchto pacientov sú do značnej miery individuálne a zohľadňujú praktické a odborné skúsenosti lekárov a analýzy doposiaľ publikovanej literatúry.
MUDr. Dušan Pávai, MPH
www.nedu.sk
Received | Doručené do redakcie | Doručeno do redakce 21. 2. 2021
Accepted | Prijaté po recenzii | Přijato po recenzi 9. 3. 2021
Received | Doručeno do redakce | Doručené do redakcie 21. 2. 2021
Accepted | Přijato po recenzi | Prijaté po recenzii 9. 3. 2021
Zdroje
- Underbjerg L, Sikjaer T, Mosekilde L et al. Pseudohypoparathyroidism – epidemiology, mortality and risk of complications. Clin Endocrinol (Oxf) 2016; 84(6): 904–911. Dostupné z DOI: <http://dx.doi.org/10.1111/cen.12948>.
- Germain-Lee EL. Management of pseudohypoparathyroidism. Curr Opin Pediatr 2019; 31(4): 537–549. Dostupné z DOI: <http://dx.doi.org/10.1097/MOP.0000000000000783>.
- Nakamura Y, Matsumoto T, Tamakoshi A at al. Prevalence of idiopathic hypoparathyroidism and pseudohypoparathyroidism in Japan. J Epidemiol 2000; 10(1): 29–33. Dostupné z DOI: <http://dx.doi.org/10.2188/jea.10.29>.
- Mantovani G, Bastepe M, Monk D et al. Diagnosis and management of pseudohypoparathyroidism and related disorders: first international Consensus Statement. Nat Rev Endocrinol 2018; 14(8): 476–500. Dostupné z DOI: <http://dx.doi.org/10.1038/s41574–018–0042–0>.
- Lemos MC, Thakker RV. GNAS mutations in Pseudohypoparathyroidism type 1a and related disorders. Hum Mutat 2015; 36(1): 11–19. Dostupné z DOI: <http://dx.doi.org/10.1002/humu.22696>.
- Eyre WG, Reed WB. Albright hereditary osteodystrophy with cutaneous bone formation. Arch Dermatol 1971; 104(6): 634–642.
- Farfel Z, Friedman E. Mentaldeficiency in pseudohypoparathyroidism type I isassociated with Ns-proteindeficiency. Ann Intern Med 1986; 105(2): 197–199. Dostupné z DOI: <http://dx.doi.org/10.7326/0003–4819–105–2-197>.
- Mallette LE, Kirkland JL, Gagel RF et al. Synthetic human parathyroid hormone-(1–34) for the study of pseudohypoparathyroidism. J Clin Endocrinol Metab 1988; 67(5): 964–972. Dostupné z DOI: <http://dx.doi.org/10.1210/jcem-67–5-964>.
- Mantovani G, Spada A, Elli FM. Pseudohypoparathyroidism and Gsalpha-cAMP-linked disorders: current view and open issues. Nat Rev Endocrinol 2016; 12(6): 347–356. Dostupné z DOI: <http://dx.doi.org/10.1038/nrendo.2016.52>.
- Linglart A, Menguy C, Couvineau A et al. Recurrent PRKAR1A mutation in acrodysostosis with hormone resistance. N Engl J Med 2011; 364(23): 2218–2226. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1012717>.
- Bringhurst FR, Demay BM, Kronenberg HM. Hormones and Disorders of Mineral Metabolism. In: Shlomo M (ed). Williams Textbook of Endocrinology. 14th ed. ELSEVIER: Philadelphia 2019 : 1242. ISBN 978–0323555968.
- Levine MA. An update on theclinical and molecular characteristics of pseudohypoparathyroidism. Curr Opin Endocrinol Diabetes Obes 2012; 19(6): 443–451. Dostupné z DOI: <http://dx.doi.org/10.1097/MED.0b013e32835a255c>.
- Tafaj O, Juppner H. Pseudohypoparathyroidism: one gene, several syndromes. J Endocrinol Invest 2017; 40(4): 347–356. Dostupné z DOI: <http://dx.doi.org/10.1007/s40618–016–0588–4>.
- Mantovani G. Clinical review: Pseudohypoparathyroidism: diagnosis and treatment. J ClinEndocrinolMetab 2011; 96(10): 3020–3030. Dostupné z DOI: <http://dx.doi.org/10.1210/jc.2011–1048>.
- Fernandez-Rebollo E, Perez de Nanclares G, Lecumberri B et al. Exclusion of the GNAS locus in PHP-Ib patients with broad GNAS methylation changes: evidence for an autosomal recessive form of PHP-Ib? J Bone Miner Res 2011; 26(8): 1854–1863. Dostupné z DOI: <http://dx.doi.org/10.1002/jbmr.408>.
- Štrbák V. Fyziológia endokrinného systemu. In: Javorka K (ed). Lekárska fyziológia. 3. prepracované a doplnené vyd. Osveta: Martin 2009 : 430–431. ISBN 9788080632915.
- Murray TM, Rao LG, Wong MM et al. Pseudohypoparathyroidism with osteitis fibrosacystica: direct demonstration of skeletal responsiveness to parathyroid hormone in cells cutured from bone. J Bone Miner Res 1993; 8(1): 83–91. Dostupné z DOI: <http://dx.doi.org/10.1002/jbmr.5650080111>.
- Chu X, Zhu Y, Wang O et al. Bone mineral density and its serial changes are associated with PTH levels in pseudohypoparathyroidism type 1B patients. J Bone Miner Res 2018; 33(4): 743–752. Dostupné z DOI: <http://dx.doi.org/10.1002/jbmr.3360>.
- Neary NM, El-Maouche D, Hopkins R et al. Development and treatment of tertiary hyperparathyroidism in patients with pseudohypoparathyroidism type 1B. J Clin Endocrinol Metab 2012; 97(9): 3025–3030. Dostupné z DOI: <http://dx.doi.org/10.1210/jc.2012–1655>.
- Park HS, Kim CG, Hong N et al. Osteosarcoma in a patient with pseudohypoparathyroidism type 1b due to paternal uniparental disomy of chromosome 20q. J Bone Miner Res 2017; 32(4): 770–775. Dostupné z DOI: <http://dx.doi.org/10.1002/jbmr.3043.
Štítky
Biochemie Dětská gynekologie Dětská radiologie Dětská revmatologie Endokrinologie Gynekologie a porodnictví Interní lékařství Ortopedie Praktické lékařství pro dospělé Radiodiagnostika Rehabilitační a fyzikální medicína Revmatologie Traumatologie OsteologieČlánek vyšel v časopise
Clinical Osteology

2021 Číslo 1
Nejčtenější v tomto čísle
- Recidivujúca hyperkalciémia – ťažký diagnostický oriešok: kazuistika
- Pseudohypoparatyreóza typu Ib: kazuistika a literárny prehľad
- Osteoporóza asociovaná s těhotenstvím: kazuistika
- Steelov syndróm – prvý prípad vzácnej kostnej dysplázie na Slovensku: kazuistika
