Vliv podkožního tuku, viscerálního tuku a objemu pánevní kosti na obsah kostních minerálů: pilotní studie na rutinních CT
Bone mineral content, subcutaneous and visceral adipose tissue volumetric measurements: A pilot study in routine computed tomography examinations
Nowadays, an increasing number of studies examine the effect of both subcutaneous and visceral fat on the quality of human life. In addition to the already proven relationship to cardiovascular disease, the question of the interrelationship between the content and quality of fatty tissue on the bone is also open. The mineral content of the pelvic bone, attenuation coefficients and volumetric values of subcutaneous and visceral fat were examined on a set of routine CT examinations of 55 patients at the University Hospital Hradec Králové. The results showed a positive relationship between fat deposits and mineral content, as well as a significant effect of overall bone size.
Keywords:
Adipose tissue – finite element method – mineral content – pelvic bone
Autoři:
Kuchař Michal 1; Morávek Alexander 1; Rejtar Pavel 2; Henyš Petr 3
Působiště autorů:
Ústav anatomie LF UK v Hradci Králové
1; Radiologická klinika LF UK a FN Hradec Králové
2; Ústav nových technologií a aplikované informatiky, Fakulta mechatroniky, informatiky a mezioborových studií, Technická univerzita v Liberci
3
Vyšlo v časopise:
Clinical Osteology 2021; 26(4): 200-208
Kategorie:
Přehledové články
Souhrn
V současné době se zvyšuje množství studií zkoumajících vliv jak podkožního, tak viscerálního tuku na kvalitu lidského života. Kromě již prokázaného vztahu ke kardiovaskulárním onemocněním je otevřena i otázka vzájemné souvislosti obsahu a kvality tukové tkáně na kost. Na souboru rutinních CT-vyšetření 55 pacientů Fakultní nemocnice Hradec Králové byl zkoumán minerální obsah pánevní kosti, atenuační koeficienty a volumetrické hodnoty podkožního a viscerálního tuku. Výsledky ukázaly kladnou souvislost mezi tukovými depozity a minerálním obsahem, zároveň naznačily zásadní vliv celkové velikosti kosti.
Klíčová slova:
tuková tkáň – metoda konečných prvků – minerální obsah – pánevní kost
Úvod
Zvýšená tělesná hmotnost člověka, případně vyšší hodnota celkového indexu tělesné hmotnosti (BMI – Body Mass Index) bývá často považována za ochranný faktor proti ztrátě kostní tkáně [1–4]. Zvyšující se mechanické namáhání indukuje anabolický efekt aktivací osteocytů a následnou expresí c-fos, IGF1 a osteokalcinu [5]. Současná akcelerace estrogenního metabolizmu ovlivňuje kostní přeměnu a výrazně zasahuje do dostupnosti vitaminu D. Přesto tuková tkáň nefunguje pouze jako prostá tělesná výplň a úložiště energie, ale i jako metabolicky aktivní orgán. Tukové buňky produkují bioaktivní proteiny, adipocytokiny, regulující řadu fyziologických procesů přímo souvisejících s tukovým metabolizmem i s onemocněními souvisejícími s obezitou, jako je diabetes 2. typu, metabolický syndrom nebo řada kardiovaskulárních onemocnění [6–15]. Leptin může svým vlivem na hypotalamus omezit novotvorbu kosti [16], v případě adiponektinu pozorujeme sníženou osteoklastogenezu [17]. Tyto negativní faktory jsou dále komplikovány jednak rozdílným zatížením různých částí těla, jednak rozdílnou kvalitou takto uložených tukových depotů. Největší z nich jsou, díky svému uložení, označovány jako podkožní tuk (SAT – Subcutaneous Adipose Tissue) a nitrobřišní tuk (VAT – Visceral Adipose Tissue). Existuje velké množství studií vycházejících z naměřených hodnot SAT a VAT, jednotlivé výsledky vlivu těchto depotů na kost, respektive kostní hustotu minerálů (BMD – Bone Mineral Density) jsou však v mnoha případech protichůdné [18–23]. V nedávno publikované metaanalýze poukázali Kaze et al na značnou heterogenitu mezi jednotlivými studiemi a doporučili další zkoumání distribuce tukových složek [24].
Chceme-li určit množství tukové tkáně v těle, můžeme využít různé antropometrické techniky (BMI, obvod pasu, poměr boků a pasu), bioelektrickou impedanční analýzu, ultrasonografii nebo data pocházející z duální rentgenové absorpciometrie/denzitometrie (DXA – Dual - -energy X-ray Absorptiometry). Žádná z těchto metod ovšem není schopná určit přesný objem a poměrné rozložení podkožního a viscerálního tuku [25]. Standardem pro hodnocení distribuce abdominálního tuku se stává výpočetní tomografie (CT – Computed Tomography) a zobrazení magnetickou rezonancí (MRI – Magnetic Resonance Imaging) s použitím různých metod a softwarových prostředků [26–29]. CT-snímky jsou zobrazeny s použitím škály Hounsfieldových jednotek (HU – Hounsfield Unit), lineární transformací všech původních měřených atenuačních koeficientů do stupňů šedi vzniká škála intenzity typická pro různé typy tkání a ve voxelech měřený objem je následně převeden do jednotek cm3.
Pro kvantifikaci lokální kostní hustoty je referenční technologií DXA [30]. Její nevýhodou je již zmíněné obtížné hodnocení volumetrických dat. Další možností je využití kvantitativní výpočetní tomografie (QCT) schopné hodnotit i volumetrická data, a tím přispět ke zlepšení predikce rizika zlomenin v porovnání s DXA [31,32]. Nedávné studie dále prokázaly možnost využití rutinních CT-skenů prováděných pro jiné než osteodenzitometrické účely, které umožňuje dostatečné kostní vyšetření bez zvýšených finančních nákladů nebo radiačního zatížení pacienta [33,34].
V této práci byl jako závislá proměnná použit obsah minerálů v kosti (BMC – Bone Mineral Content) místo BMD. Ačkoliv bývá BMD používána častěji a je obecně uznávána jako měřítko stupně osteopenie a osteoporózy, neodráží dostatečně vliv velikosti kosti [35]. Měření DXA ze svého principu mohou přecenit hodnotu kostní hustoty u pacientů s malými kostmi, nebo naopak podcenit tuto hodnotu u pacientů s kostmi absolutně většími. BMC je hmotnost minerální složky kosti a je počítána z celého objemu kosti na základě CT-snímků.
Cíl studie
Cílem studie bylo vyhodnotit vliv podkožního tuku, viscerálního tuku a nově i objemu kosti na množství minerálních látek za použití volumetrických dat z rutinních CT-vyšetření. Práce byla zaměřena na náhodně vybranou skupinu dospělých osob ve věku do 60 let.
Materiál a metodika
Soubor dat
Anonymizovaná retrospektivní data z CT-vyšetření 28 mužů a 27 žen byla náhodně vybrána ze souboru rutinních vyšetření provedených ve Fakultní nemocnici Hradec Králové. Rozlišení snímků bylo 1 × 1 × 1 mm (Siemens Definition AS+ a Siemens Definiton 128, Siemens AG, Erlangen, Germany; 120–130 kV; CareDose, reconstruction kernel 80–90, bone algorithm). Vstupní kritéria byla: abdominální CT, věk mezi 24–60 lety a pánevní kosti bez zjevného traumatu. Výběr pacientů proběhl s cílem doplnit současné studie o náhodný vzorek populace středního věku. Většina studií se zaměřuje na skupiny osob mladších, starších, prokazatelně obézních nebo na soubory s širokým věkovým rozptylem [36–41]. Přes pochopitelné důvody k výběru těchto skupin je v dostupné literatuře velmi málo informací o změnách minerálního obsahu u osob středního věku. Vybrané věkové rozmezí by mělo zároveň potlačit vliv hormonálních změn na kosti v období menopauzy u žen.
Obsah kostního minerálu
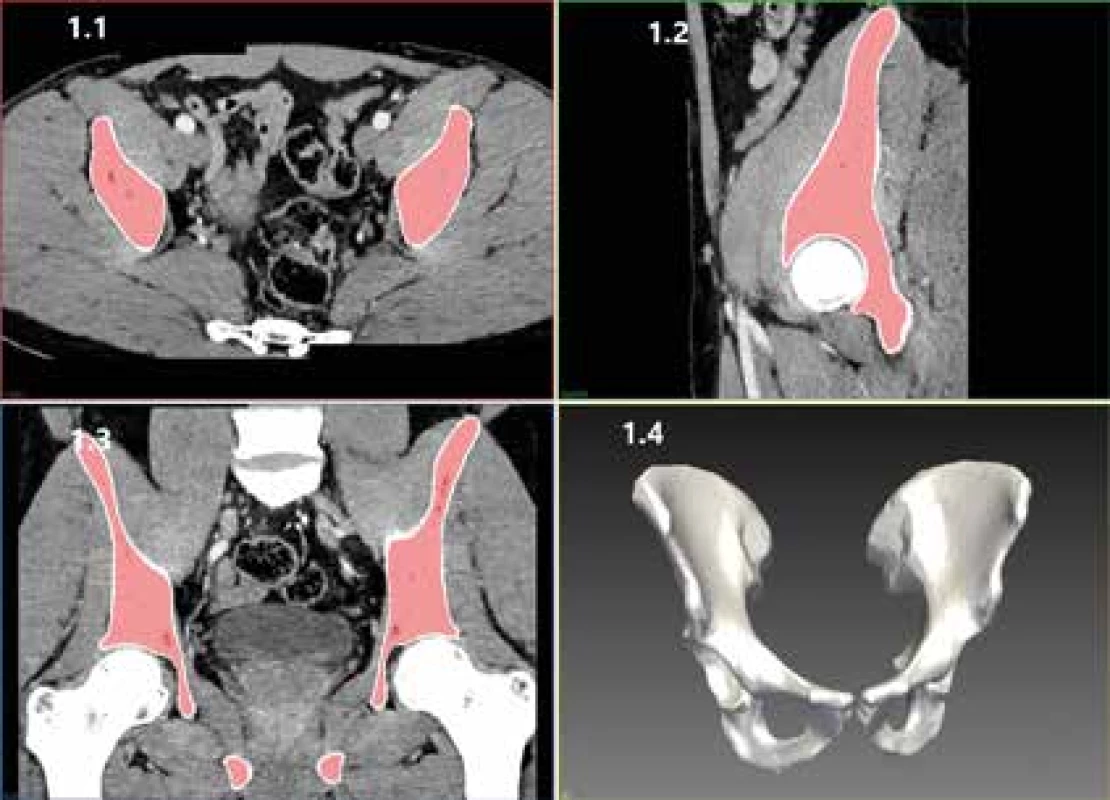
Geometrie pánevních kostí byla extrahována s použitím MITK-GEM interaktivního segmentačního software [42]. Nejdříve byly na několika snímcích manuálně naznačeny hrubé kontury kosti a pozadí, následně GraphCut algoritmus vysegmentoval zbytek řezů (obr. 1). Vzhledem k tomu, že se jedná o retrospektivní studii založenou na rutinních CT, nebyl k dispozici fantom pro kalibraci jednotek HU na jednotky minerální hustoty kosti. Proto byla v této studii aplikována metoda takzvané „interní kalibrace“ podle studie Michalskiho [43]. Tato metodika je založená na tom, že atenuační koeficienty vybraných typů tkání nejsou citlivé na konfiguraci CT-přístroje. Tyto koeficienty uvádějí Looker et al a Scott [44,45]. Autoři tento typ kalibrace ověřili a demonstrovali v předchozích publikacích [46,47]. Po kalibraci je výsledné pole hodnot HU převedeno na hustotu hydroxyapatitu HA v [g/cm3].
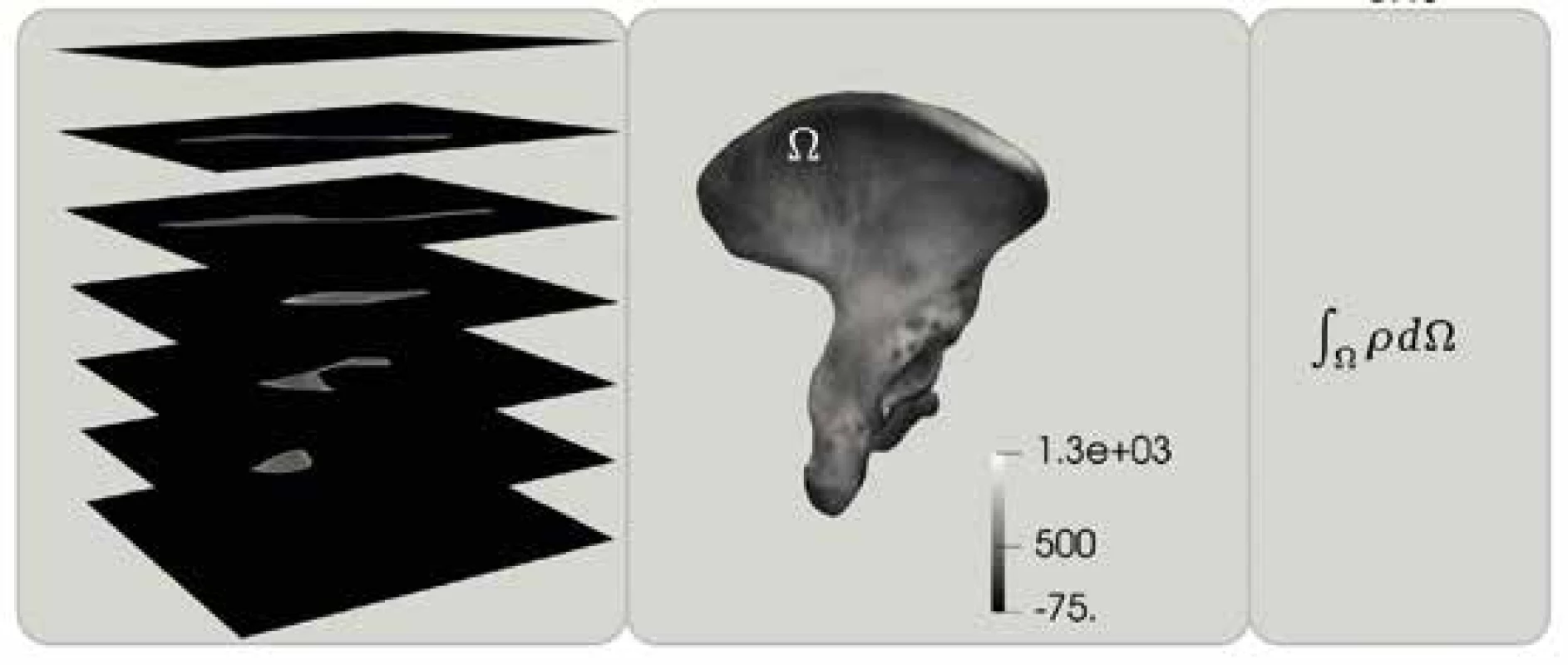
Minerální hmotnost kosti (BMC) byla spočítána následujícím způsobem. Nejdříve byla extrahována prostorová geometrie jako výsledek segmentace, tj. povrch ve formátu stl (viz výše) a minerální hustota kosti z CT - -řezů. Hustota kosti je v každém místě kosti různá, a proto je hmotnost kosti dána jako integrál, který lze spočítat jenom numericky (viz předchozí práce autorů), obr. 2. Ve studii [47] počítali autoři BMC pomocí metody konečných prvků (MKP), která se hojně používá v biomechanice [48].
Nicméně autoři této studie dále studovali hmotnost kosti tak, že je zajímal podíl vlivu objemu kosti a minerální hustoty na výslednou hmotnost kosti. Tato separace není triviální a autoři se inspirovali v předchozích studiích algoritmem, který se používá v analýze MRI mozku a k normalizaci tvaru mozku. Tato separace znamená, že se tvar kosti transformuje na jistý průměrný tvar (šablonu), ale hustota kosti zůstane zachována. Tato transformace je počítána pomocí algoritmu SyN knihovny ANTs. Vhodné nastavení tohoto algoritmu pro kostní tkáň a jeho přesnost byla demonstrována v předchozí publikaci stejných autorů [49], stejně jako odhad průměrného tvaru kosti. Touto transformací je dosaženo toho, že všichni pacienti mají stejný tvar kosti (jak ženy, tak muži), a tudíž je vliv tvaru na výslednou minerální hmotnost potlačen. Ve studii je rozlišeno BMCa spočítané na průměrné kosti a BMCi individuálního pacienta.
Analýza tukové tkáně
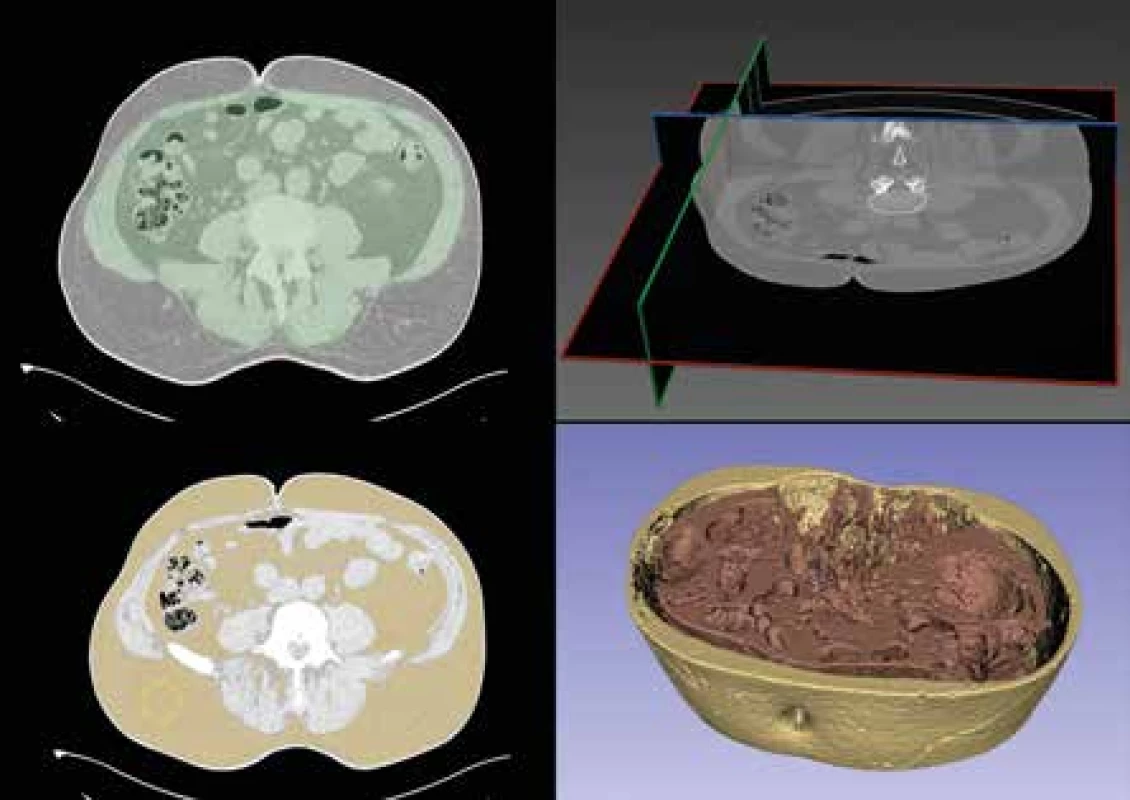
Pro výpočet celkového objemu VAT a SAT, z každého vyšetření byl ručně vybrán blok v oblasti břicha o délce 10 cm (100 řezů) s centrem v umbiliku. Tato úroveň by měla pokrývat jak nejčastěji používaný antropometrický rozměr (obvod břicha [50]), tak obratel L4, v literatuře opakovaně používaný pro kvantitativní hodnocení poměru VAT/SAT [21,51]. Snímky byly načteny a zpracovány v programu 3DSlicer [52] s ručním vyznačením pozice abdominální fascie na několika řezech a následným automatickým vyznačením v rámci celého bloku (obr. 3.1, obr. 3.2). Program dále umožňuje využít virtuální štětec a po zakreslení plochy do oblasti jednoho z tukových depotů změřit ve vybrané oblasti rozsah jednotek HU definujících tukovou tkáň (obr. 3.3). Tento individuální rozsah HU byl poté aplikován na všechny řezy daného CT. Po automatické segmentaci peritoneální dutiny včetně okolních svalů (intraabdominální prostor – IA) a následné manuální korekci byla hodnota SAT definována jako celkový objem tukové tkáně mezi kůží břicha a vnějším okrajem břišních a paravertebrálních svalů. Objem VAT byl definován a kvantifikován podle Sheu et al [20] jako souhrn voxelů uvnitř výše zmíněné hranice, z nichž žádný nepatřil ke svalové tkáni nebo k vnitřním orgánům (obr. 3.4). Z tohoto objemu jsme zároveň odvodili průměrnou hodnotu HU pro VAT i SAT.
Prostorová závislost SAT, VAT
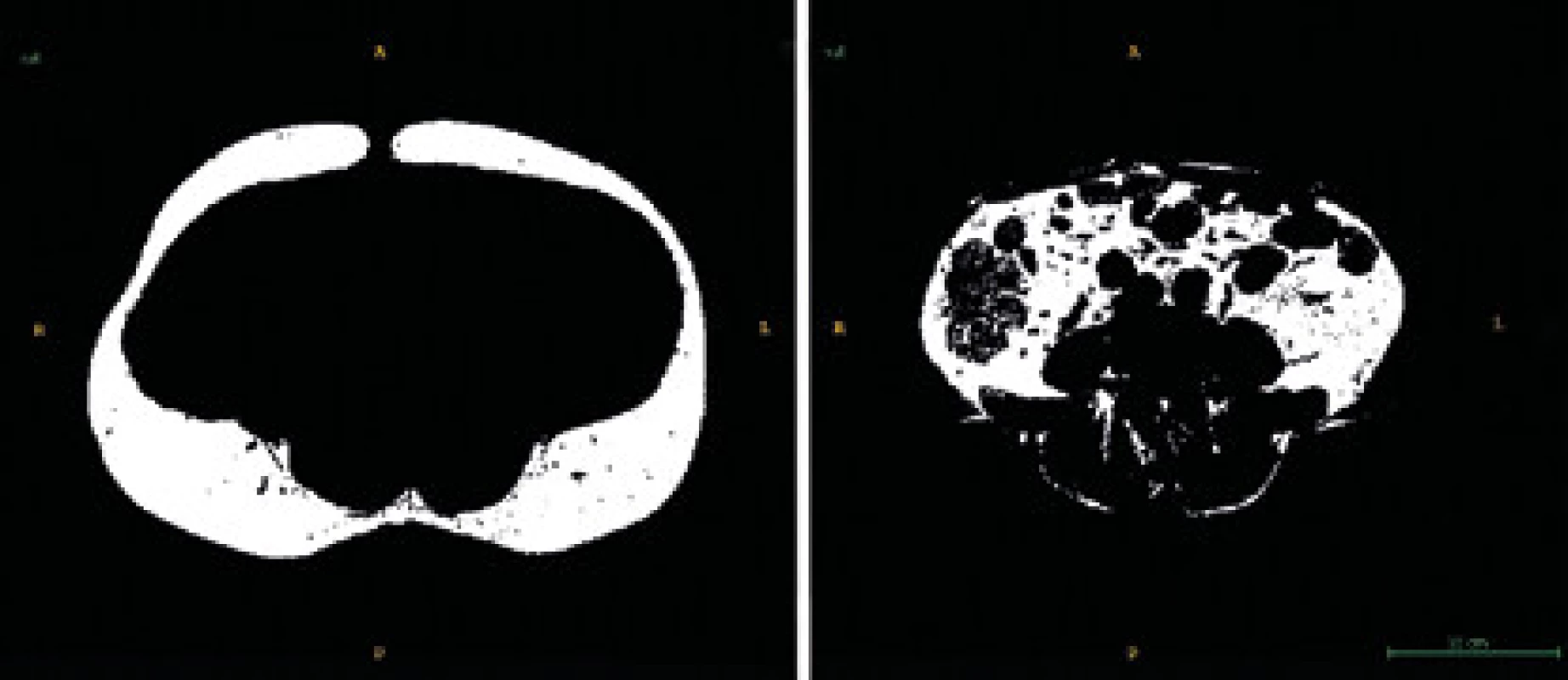
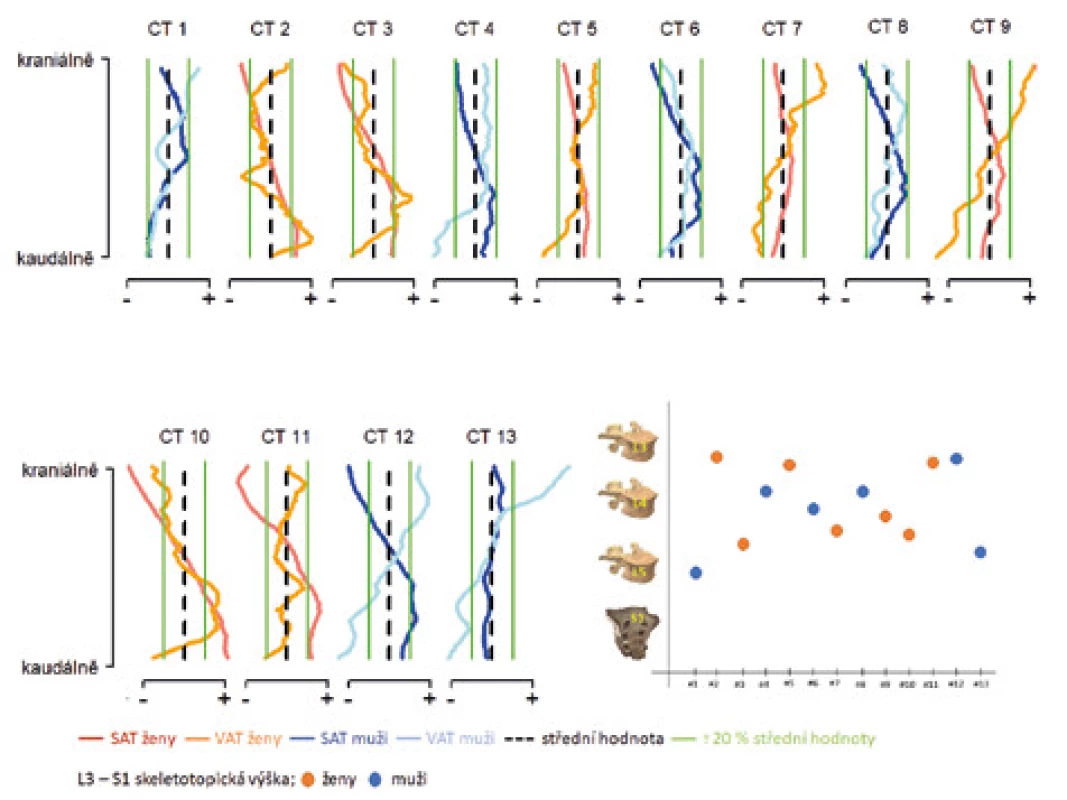
U náhodně vybraných 13 pacientů byl s použitím předchozí segmentace v každém z jejich axiálních řezů nezávisle vyznačen prostor zaplněný podkožním a viscerálním tukem. Obsahy každého z řezů, stejně jako jejich vzájemné poměry, byly následně spočítány automaticky a jejich rozložení graficky zvýrazněno. Při daném rozlišení tedy vzniklo 100 snímků pro danou osobu, popisujících kranio-kaudální rozložení tukové tkáně v části břišní dutiny (obr. 4).
Statistické zhodnocení
Pro zhodnocení rozložení tukových složek jsme použili grafické hodnocení, pro porovnání množství BMC a jeho souvislosti s tukovými složkami byl využit Pearsonův korelační koeficient.
V případě grafického hodnocení byla každá z tukových složek na individuální úrovni normalizovaná na jednotkový průměr způsobem, při němž byly původní hodnoty děleny průměrem dané veličiny. Tím bylo dosaženo vzájemné grafické srovnatelnosti veličin s řádově rozdílným rozložením hodnot. Před provedením samotné korelace byla testována normalita rozložení hodnot pomocí jednovýběrového Kolmogorovova-Smirnovova testu, jenž porovnává rozložení naměřených hodnot vůči teoretickému rozložení. V našem případě bylo teoretické rozložení tvořeno nově vygenerovaným normálním rozdělením se střední hodnotou a rozptylem odpovídajícími původním datům, přičemž byl zachován počet prvků. Samotná síla vztahu mezi jednotlivými proměnnými byla zkoumána prostřednictvím Pearsonova korelačního koeficientu lineární závislosti.
Pro hodnocení obsahu minerálních látek v kosti byla korigována proměnná BMCa, ve které byl odstraněn klesající trend obsahu minerálních látek v kosti s narůstajícím věkem. Korekce byla získána zpětnou aplikací regresní rovnice BMCa na věk, přičemž k reziduím (rozdíl původních hodnot BMCa a nových odhadů této veličiny) byla připočtena průměrná hodnota těchto odhadů.
Výsledky a diskuse
Z důvodu časové a finanční náročnosti používá většina studií k hodnocení vlivu podkožního a viscerálního tuku hodnoty odvozené z jednoho nebo jen několika řezů. Ačkoliv můžeme v dostupné literatuře najít práce prokazující závislost mezi celkovým objemem tukové tkáně a jen několika snímky. Vzhledem k populační variabilitě pacientů musíme být v tomto případě velmi opatrní. Pozice, velikost i náplň okolních orgánů budou výrazně ovlivňovat celkové množství tuku v abdominální dutině. Oproti relevantním studiím jsme přes menší počet zahrnutých subjektů poprvé hodnotili oblast břicha v souvislé řadě 1 mm řezů. V našem případě ukázalo porovnání obsahu viscerálního a podkožního tuku na jejich nerovnoměrné rozložení (obr. 5). V centrální části vytvořeného bloku je shoda s celkovou střední hodnotou největší, přesto se v porovnání s doporučovanou skeletotopickou výškou L4 (která nemusí souviset se středem výřezu) lišil absolutní průměr od průměrného obsahu v této rovině jak pro SAT (5–27 procent), VAT (4–56 procent) i VAT/SAT (0,5–110 procent).
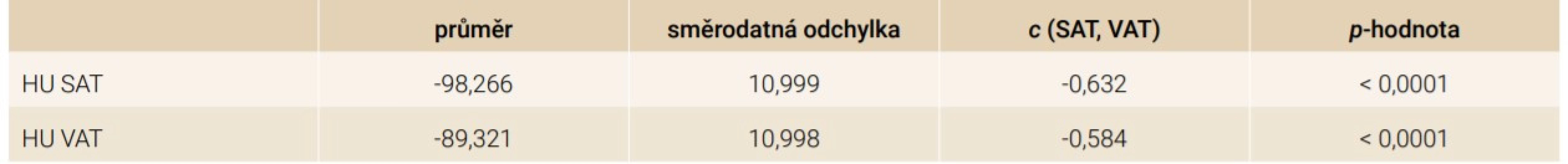
Některé z námi naměřených hodnot potvrdily dosud publikované výsledky. Stejně jako ve studiích Baby a Hu [53,54] jsme nalezli silnou korelaci mezi množstvím SAT i VAT a jejich průměrnou hodnotou Hounsfieldových jednotek (tab. 1). V tomto případě se zdá, že i samotná kvalita tukové tkáně může být důležitým diagnostickým znakem –předpokládá se, že nižší hodnota HU je asociována s vyšším obsahem lipidů. Absolutně větší množství tukové tkáně jsme nalezli u žen, ovšem s jiným rozložením než u mužů. Zcela převládá složka SAT, stejně jako poměr SAT/VAT. U mužů převládá množství viscerálního tuku a poměr VAT/SAT (tab. 2). U obou pohlaví se s přibývajícím věkem zvyšuje množství viscerálního tuku, u podkožního tuku jsme tento trend v námi zkoumaném souboru nepozorovali (tab. 3).
Průměrný minerální obsah jsme měřili v rozsahu celých pánevních kostí. Ačkoliv se nejedná o cílenou strukturu pro běžná denzitometrická vyšetření, díky svému velkému objemu, relativně snadné segmentaci a současné dostupnosti abdominálních CT se zdá vhodným cílem pro následné porovnání s dalšími veličinami. Absolutní hodnoty SAT a VAT byly použity jako vstupní data a jen nepřímo odkazují na robustnost postavy pacienta, kterou jsme díky nedostupnosti dalších vyšetření (tělesná hmotnost, BMI) nebyli schopni odfiltrovat. Následně vytvořené poměry tukových složek a částí břišní oblasti lépe odrážejí celkovou topografii a jsou nezávislé na tělesné stavbě.
Hodnota BMCi vykazovala středně silnou korelaci s příslušností k jednotlivému pohlaví a celkovým objemem břišního bloku (p < 0,001), s hodnotou VAT i SAT + VAT u mužů (p = 0,03; 0,021) a SAT u žen (p = 0,037). Jednotlivé poměry tukových složek se u žen ukázaly jako méně významné, u mužů záviselo na poměru VAT k objemu břišní dutiny i k celému objemu břišní oblasti (tab. 4).
Zajímavá situace však nastala po převedení BMCi na BMCa, při kterém se namapováním celé kosti včetně minerálního obsahu na univerzální šablonu odfiltroval vliv její velikosti. Jinými slovy vidíme, jak by vypadala kost se stejným rozložením minerální složky po převedení na jednotný tvar. Po použití tohoto typu dat (BMCa) zcela vymizel vliv pohlaví na obsah kostních minerálů (tab. 3). Je tedy možné, že pozorované pohlavní rozdíly u řady denzitometrických studií mohou být ovlivněné převážně rozdílnou velikostí jednotlivých kostí a až sekundárně jinými pohlavně specifickými vlivy. Tento přepočet nám umožnil použít celý smíšený soubor pacientů. Zde jsme opět nalezli souvislost minerálního obsahu kosti s absolutním objemem měkkých tkání a s poměry VAT (tab. 4). V žádném z případů (BMCi, BMCa) se neprokázala souvislost s indexem podkožního a viscerálního tuku (VAT/ SAT).
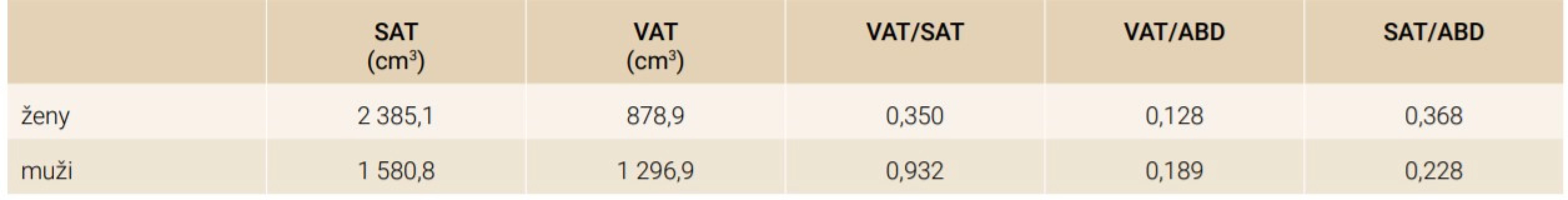
ABD – objem celého břišního bloku
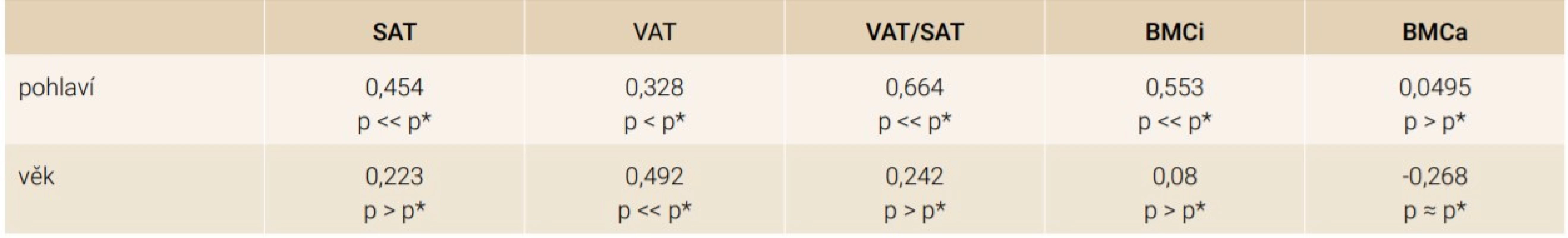
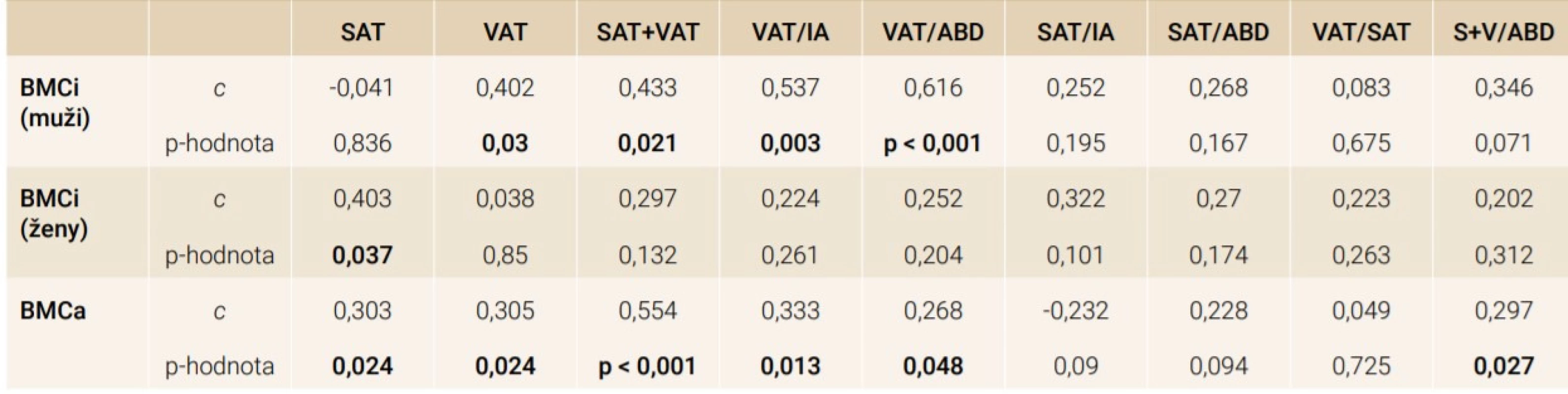
Úzký vztah BMC k měřeným objemům pravděpodobně z velké části souvisí s celkovou tělesnou konstitucí, a tím i tlakem na pánevní kosti. Vzhledem k potvrzené souvislosti BMCa k poměrům tukových složek však můžeme předpokládat i vliv dalších faktorů nezávislých na hmotnosti. U žen jsme nalezli větší význam podkožního tuku, u mužů viscerálního, ve všech případech jeho zvýšenou hodnotu následovalo zvýšení BMC.
Jsme si vědomi, že znalost minerálního obsahu je pouze jednou ze složek vyšetření a celková hodnota může být zkreslena lokální nižší metabolickou aktivitou nebo právě rozdílnou velikostí kosti a nemusí odpovídat její celkové kvalitě. Zároveň jsou tyto výsledky úzce svázány s vybranou věkovou skupinou osob mladších 60 let. Ačkoliv nepředpokládáme výrazné změny při působení tukových výplní na jiné části skeletu, vzhledem k rozdílným poměrům kortikální a trabekulární kosti je nezbytné budoucí porovnání s kostmi běžnými pro denzitometrická vyšetření, jako jsou obratle či proximální část stehenní kosti.
Závěr
Na náhodně vybraném souboru osob středního věku jsme hledali souvislost mezi velikostí kosti, jejím minerálním obsahem a tukovými depozity ve vybrané části břišní oblasti. Nalezli jsme kladnou souvislost mezi objemem tuků a jejich průměrnými atenuačními koeficienty, dále mezi absolutním i relativním množstvím tukové tkáně a BMC. Poměr viscerálního k podkožnímu tuku se v našem souboru ukázal jako nevýznamný. Prokázali jsme silnější závislost BMC na objemu kosti, než na pohlavní specificitě. Přesnější interpretace výsledků, včetně začlenění dalších typů kostí, bude součástí dalšího výzkumu.
Received | Doručeno do redakce | Doručené do redakcie 30. 6. 2021
Accepted | Přijato po recenzi | Prijaté po recenzii 27. 7. 2021
Alexander Morávek | moravekal@lfhk.cuni.cz | www.lfhk.cuni.cz
Zdroje
- Wardlaw GM. Putting body weight and osteoporosis into perspective. Am J Clin Nutr 1996; 63(3 Suppl): 433S-436S. Dostupné z DOI: <http://dx.doi.org/10.1093/ajcn/63.3.433>.
- Edelstein SL, Barrett-Connor E. Relation between Body-Size and Bone-Mineral Density in Elderly Men and Women. Am J Epidemiol 1993; 138(3): 160–169. Dostupné z DOI: <http://dx.doi.org/10.1093/ oxfordjournals.aje.a116842>.
- Reid IR. Relationships among body mass, its components, and bone. Bone 2002; 31(5): 547–555. Dostupné z DOI: <http://dx.doi. org/10.1016/s8756–3282(02)00864–5>.
- Reid IR, Ames R, Evans MC et al. Determinants of Total-Body and Regional Bone-Mineral Density in Normal Postmenopausal Women – a Key Role for Fat Mass. J Clin Endocrinol Metab 1992; 75(1): 45–51. Dostupné z DOI: <http://dx.doi.org/10.1210/jcem.75.1.1619030>.
- Zhao LJ, Jiang H, Papasian CJ et al. Correlation of obesity and osteoporosis: Effect of fat mass on the determination of osteoporosis. J Bone Miner Res 2008; 23(1): 17–29. <http://dx.doi.org/10.1359/ jbmr.070813>.
- Matsuzawa Y. The metabolic syndrome and adipocytokines. Febs Letters 2006; 580(12): 2917–2921. Dostupné z DOI: <http://dx.doi.org/10.1016/j.febslet.2006.04.028>.
- Matsuzawa Y. Therapy insight: adipocytokines in metabolic syndrome and related cardiovascular disease. Nat Clin Pract Cardiovasc Med 2006; 3(1): 35–42. Dostupné z DOI: <http://dx.doi.org/10.1038/ ncpcardio0380>.
- Matsuzawa Y. Adiponectin: A Key Player in Obesity Related Disorders. Curr Pharm Des 2010; 16(17): 1896–1901. Dostupné z DOI: <http://dx.doi.org/10.2174/138161210791208893>.
- Hotamisligil GS, Shargill NS, Spiegelman BM. Adipose Expression of Tumor-Necrosis-Factor-Alpha – Direct Role in Obesity-Linked Insulin Resistance. Science 1993; 259(5091): 87–91. Dostupné z DOI: <http://dx.doi.org/10.1126/science.7678183>.
- Matsuzawa Y. Adiponectin: Identification, physiology and clinical relevance in metabolic and vascular disease. Atheroscler Suppl 2005; 6(2): 7–14. Dostupné z DOI: <http://dx.doi.org/10.1016/j.atherosclerosissup.2005.02.003>.
- Shimomura I, Funahashi T, Takahashi M et al. Enhanced expression of PAI-1 in visceral fat: Possible contributor to vascular disease in obesity. Nat Med 1996; 2(7): 800–803. Dostupné z DOI: <http:// dx.doi.org/10.1038/nm0796–800>.
- Steppan CM, Bailey ST, Bhat S et al. The hormone resistin links obesity to diabetes. Nature 2001; 409(6818): 307–312. Dostupné z DOI: <http://dx.doi.org/10.1038/35053000>.
- Hug C, Lodish HF. Visfatin: A new adipokine. Science 2005; 307(5708): 366–367. Dostupné z DOI: <http://dx.doi.org/10.1126/science.1106933>.
- Ritchie SA, Connell JM. The link between abdominal obesity, metabolic syndrome and cardiovascular disease. Nutr Metab Cardiovasc Dis 2007; 17(4): 319–326. Dostupné z DOI: <http://dx.doi.org/10.1016/j.numecd.2006.07.005>.
- Pinthus JH, Kleinmann N, Tisdale B et al. Lower Plasma Adiponectin Levels Are Associated with Larger Tumor Size and Metastasis in Clear-Cell Carcinoma of the Kidney. Eur Urol 2008; 54(4): 866–873. Dostupné z DOI: <http://dx.doi.org/10.1016/j.eururo.2008.02.044>.
- Ducy P, Amling M, Takeda S et al. Leptin inhibits bone formation through a hypothalamic relay: A central control of bone mass. Cell 2000; 100(2): 197–207. Dostupné z DOI: <http://dx.doi.org/10.1016/ s0092–8674(00)81558–5>.
- Williams GA, Wang Y, Callon KE et al. In Vitro and in Vivo Effects of Adiponectin on Bone. Endocrinology 2009; 150(8): 3603–3610. Dostupné z DOI: <http://dx.doi.org/10.1210/en.2008–1639>.
- Cawthon PM, Shahnazari M, Orwoll ES et al. Osteoporosis in men: findings from the Osteoporotic Fractures in Men Study (MrOS). Ther Adv Musculoskelet Dis 2016; 8(1): 15–27. Dostupné z DOI: <http:// dx.doi.org/10.1177/1759720X15621227>.
- Nielson CM, Marshall LM, Adams AL et al. BMI and Fracture Risk in Older Men: The Osteoporotic Fractures in Men Study (MrOS). J Bone Miner Res 2011; 26(3): 496–502. Dostupné z DOI: <http://dx.doi. org/10.1002/jbmr.235>.
- Sheu Y, Marshall ML, Holton KF et al. Abdominal body composition measured by quantitative computed tomography and risk of non - -spine fractures: the Osteoporotic Fractures in Men (MrOS) study. Osteoporos Int 2013; 24(8): 2231–2241. Dostupné z DOI: <http://dx.doi. org/10.1007/s00198–013–2322–9>.
- Sollmann N, Franz D, Burian E et al. Assessment of paraspinal muscle characteristics, lumbar BMD, and their associations in routine multi-detector CT of patients with and without osteoporotic vertebral fractures. Eur J Radiol 2020; 125 : 108867. Dostupné z DOI: <http:// dx.doi.org/10.1016/j.ejrad.2020.108867>.
- Russell M, Mendes N, Miller KK et al. Visceral Fat Is a Negative Predictor of Bone Density Measures in Obese Adolescent Girls. J Clin Endocrinol Metab 2010; 95(3): 1247–1255. Dostupné z DOI: <http:// dx.doi.org/10.1210/jc.2009–1475>.
- de Paula FJ, de Araújo IM, Carvalho AL et al. The Relationship of Fat Distribution and Insulin Resistance with Lumbar Spine Bone Mass in Women. PLoS One 2015; 10(6): e0129764. Dostupné z DOI: <http:// dx.doi.org/10.1371/journal.pone.0129764>.
- Kaze AD, Rosen HN, Paik JM. A meta-analysis of the association between body mass index and risk of vertebral fracture. Osteoporos Int 2018; 29(1): 31–39. <http://dx.doi.org/10.1007/s00198–017 – 4294–7>.
- Shuster A, Patlas M, Pinthus JH et al. The clinical importance of visceral adiposity: a critical review of methods for visceral adipose tissue analysis. Br J Radiol 2012; 85(1009): 1–10. Dostupné z DOI: <http://dx.doi.org/10.1259/bjr/38447238>.
- Seidell JC, Bakker CJ, Vanderkooy K. Imaging Techniques for Measuring Adipose-Tissue Distribution – a Comparison between Computed-Tomography and 1.5-T Magnetic-Resonance. Am J Clin Nutr 1990; 51(6): 953–957. Dostupné z DOI: <http://dx.doi.org/10.1093/ ajcn/51.6.95>.
- Direk K, Cecelja M, Astle W et al. The relationship between DXA - -based and anthropometric measures of visceral fat and morbidity in women. BMC Cardiovasc Disord 2013; 13 : 25. Dostupné z DOI: <http:// dx.doi.org/10.1186/1471–2261–13–25>
- Jensen MD, Kanaley JA, Reed JE et al. Measurement of Abdominal and Visceral Fat with Computed-Tomography and Dual-Energy X-Ray Absorptiometry. Am J Clin Nutr 1995; 61(2): 274–278. Dostupné z DOI: <http://dx.doi.org/10.1093/ajcn/61.2.274>
- Jensen MD, Kanaley JA, Roust LR et al. Assessment of Body - -Composition with Use of Dual-Energy X-Ray Absorptiometry – Evaluation and Comparison with Other Methods. Mayo Clin Proc 1993; 68(9): 867–873. Dostupné z DOI: <http://dx.doi.org/10.1016/s0025 – 6196(12)60695–8>.
- Loffler MT, Sollmann N, Mei K et al. X-ray-based quantitative osteoporosis imaging at the spine. Osteopor Int 2020 31(2): 233–250. Dostupné z DOI: <http://dx.doi.org/10.1007/s00198–019–05212–2>.
- Engelke K. Quantitative Computed Tomography-Current Status and New Developments. J Clin Densitom 2017; 20(3): 309–321. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jocd.2017.06.017>.
- Loffler MT, Jacob A, Valentinitsch A et al. Improved prediction of incident vertebral fractures using opportunistic QCT compared to DXA. Eur Radiol 2019; 29(9): 4980–4989. Dostupné z DOI: <http:// dx.doi.org/10.1007/s00330–019–06018-w>.
- Winsor C, Qasim M, Henak CR et al. Evaluation of patient tissue selection methods for deriving equivalent density calibration for femoral bone quantitative CT analyses. Bone 2021; 143 : 115759. Dostupné z DOI: <http://dx.doi.org/10.1016/j.bone.2020.115759>.
- Tse JJ, Smith AC, Kuczynski MT et al. Advancements in Osteoporosis Imaging, Screening, and Study of Disease Etiology. Curr Osteoporos Rep 2021; 19(5): 532–541. Dostupné z DOI: <http://dx.doi. org/10.1007/s11914–021–00699–3>.
- Prentice A, Parsons TJ, Cole TJ. Uncritical Use of Bone-Mineral Density in Absorptiometry May Lead to Size-Related Artifacts in the Identification of Bone-Mineral Determinants. Am J Clin Nutr 1994; 60(6): 837–842. Dostupné z DOI: <http://dx.doi.org/10.1093/ ajcn/60.6.837>.
- Afghani A, Goran MI. Racial differences in the association of subcutaneous and visceral fat on bone mineral content in prepubertal children. Calcif Tissue Int 2006;79(6): 383–388. Dostupné z DOI: <http:// dx.doi.org/10.1007/s00223–006–0116–1>.
- Glass NA, Torner JC, Letuchy EM et al. Does Visceral or Subcutaneous Fat Influence Peripheral Cortical Bone Strength During Adolescence? A Longitudinal Study. J Bone Miner Res 2018; 33(4): 580–588. Dostupné z DOI: <http://dx.doi.org/10.1002/jbmr.3325>.
- Crivelli M, Chain A, da Silva IT et al. Association of Visceral and Subcutaneous Fat Mass With Bone Density and Vertebral Fractures in Women With Severe Obesity. J Clin Densitom 2021; 24(3): 397–405. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jocd.2020.10.005>.
- El Hage R, Jacob C, Moussa E et al. Relative importance of lean mass and fat mass on bone mineral density in a group of Lebanese postmenopausal women. J Clin Densitom 2011; 14(3): 326–331. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jocd.2011.04.002>
- Ryl A, Rotter I, Szylińska A et al. Complex interplay among fat, lean tissue, bone mineral density and bone turnover markers in older men. Aging (Albany NY) 2020; 12(19): 19539–19545. Dostupné z DOI: <http://dx.doi.org/10.18632/aging.103903>.
- Kim JH, Choi HJ, Kim MJ et al. Fat mass is negatively associated with bone mineral content in Koreans. Osteoporos Int 2012; 23(7): 2009–2016. Dostupné z DOI: <http://dx.doi.org/10.1007/s00198 – 011–1808–6>.
- Pauchard Y, Fitze T, Browarnik D et al. Interactive graph-cut segmentation for fast creation of finite element models from clinical ct data for hip fracture prediction. Comput Methods Biomech Biomed Engin 2016; 19(16): 1693–1703. Dostupné z DOI: <http://dx.doi.org10.1 080/10255842.2016.1181173>.
- Michalski AS, Besler BA, Michalak GJ et al. CT-based internal density calibration for opportunistic skeletal assessment using abdominal CT scans. Med Eng Phys 2020; 78 : 55–63. Dostupné z DOI: <http:// dx.doi.org/10.1016/j.medengphy.2020.01.009>
- Looker AC, Borrud LG, Hughes JH et al. Total body bone area, bone mineral content, and bone mineral density f or individuals aged 8 years and over: United States, 1999–2006. Vital Health Stat 2013; 11(253): 1–78.
- Scott JA. Photon, Electron, Proton and Neutron Interaction Data for Body Tissues: ICRU Report 46. International Commission on Radiation Units and Measurements, Bethesda 1992. Soc Nuclear Med/J Nuclear Med 1993.
- Henyš P, Vořechovský M, Kuchař M et al. Bone mineral density modeling via random field: normality, stationarity, sex and age dependence. Comput Methods Programs Biomed 2021; 210 : 106353. Dostupné z DOI: <http://dx.doi.org/10.1016/j.cmpb.2021.106353>.
- Henyš P, Kuchař M, Hájek P et al. Mechanical metric for skeletal biomechanics derived from spectral analysis of stiffness matrix. Sci Rep 2021; 11(1): 15690. Dostupné z DOI: <http://dx.doi.org/10.1038/ s41598–021–94998–5>.
- Taylor M, Prendergast PJ. Four decades of finite element analysis of orthopaedic devices: where are we now and what are the opportunities? J Biomech 2015; 48(5): 767–778. Dostupné z DOI: <http://dx.doi. org/10.1016/j.jbiomech.2014.12.019>.
- Kuchar M, Henyš P, Rejtar P et al. Shape morphing technique can accurately predict pelvic bone landmarks. Int J Legal Med 2021; 135(4): 1617–1626. Dostupné z DOI: <http://dx.doi.org/10.1007/ s00414–021–02501–6>
- Ball SD, Swan PD. Accuracy of estimating intra-abdominal fat in obese women. JEPonline 2003; 6(4):1–7.
- Hassan EB, Demontiero O, Vogrin S et al. Marrow Adipose Tissue in Older Men: Association with Visceral and Subcutaneous Fat, Bone Volume, Metabolism, and Inflammation. Calcif Tissue Int 2018; 103(2): 164–174. Dostupné z DOI: <http://dx.doi.org/10.1007/s00223–018 – 0412–6>.
- Pieper S, Halle M, Kikinis R. 3D Slicer. 2004 2nd IEEE International Symposium on Biomedical Imaging: Nano to Macro (IEEE Cat No. 04EX821). VOLs 1 and 2, 2004 : 632–635. Dostupné z DOI: <http://doi: 10.1109/isbi.2004.1398617 Corpus ID: 228577>.
- Baba S, Jacene HA, Engles JM et al. CT Hounsfield units of brown adipose tissue increase with activation: preclinical and clinical studies. J Nucl Med 2010; 51(2): 246–250. Dostupné z DOI: <http://dx.doi. org/10.2967/jnumed.109.068775>.
- Houchun HH, Chung SA, Nayak KS et al. Differential computed tomographic attenuation of metabolically active and inactive adipose tissues: preliminary findings. J Comput Assist Tomogr2011; 35(1): 65–71. Dostupné z DOI: <http://dx.doi.org/10.1097/ RCT.0b013e3181fc2150>.
Štítky
Biochemie Dětská gynekologie Dětská radiologie Dětská revmatologie Endokrinologie Gynekologie a porodnictví Interní lékařství Ortopedie Praktické lékařství pro dospělé Radiodiagnostika Rehabilitační a fyzikální medicína Revmatologie Traumatologie OsteologieČlánek vyšel v časopise
Clinical Osteology

2021 Číslo 4
Nejčtenější v tomto čísle
- Atypické fraktury femuru – co je nového?
- Vliv podkožního tuku, viscerálního tuku a objemu pánevní kosti na obsah kostních minerálů: pilotní studie na rutinních CT
- Péče o pacienty s osteoporózou v období pandemie COVID-19
- Doplnění sborníku abstrakt: XXIV. mezinárodní kongres českých a slovenských osteologů
